گلوکوز
گلوکوز شوگر کی ایک قسم ہے جس کا کیمیائی فارمولا
C6H12O6 ہوتا ہے۔ ساری شوگروں کی طرح گلوکوز بھی کاربوہائیڈریٹ کے خاندان سے تعلق رکھتا ہے۔ گلوکوز کو dextrose یا بلڈ شوگر بھی کہتے ہیں۔ یہ انگور چینی کے طور پر بھی جانا جاتا ہے۔ یہ ایک سادہ چینی (monosaccharide) ہے اور حیاتیات میں ایک نہایت اہم کاربوہائڈریٹ ہے کیونکہ خلیات اس سے توانائی حاصل کرتے ہیں۔ گلوکوز پودوں میں ضیائی تالیف کے نتیجے میں سورج کی توانائی جذب کر کے بنتا ہے اور مختلف جانداروں میں عمل اندرونی تنفس کے نتیجے میں ٹوٹ کر اپنی توانائی جاندار کو مہیا کرتا ہے۔
انسان اور جانوروں کے جسم میں ضرورت سے زیادہ گلوکوز کے مولیکیول باہم جُڑ کر glycogen کی شکل اختیار کر لیتے ہیں جو بلڈ شوگر بڑھائے بغیر جسم میں ذخیرہ کیا جا سکتا ہے۔ یہاں گلوکوز ایک مونومر ہے جبکہ اس سے بنا گلائیکوجن ایک پولی مر ہے۔ اس کے بر عکس پودے اپنا زائد گلوکوز اسٹارچ (نشاستے) کی شکل میں ذخیرہ کرتے ہیں جو گلائیکوجن کی طرح گلوکوز کا ایک دوسرا پولی مر ہوتا ہے۔ جب غذا کی قلت ہوتی ہے تو جانور اپنے گلائیکوجن سے اور پودے اپنے نشاستے سے دوبارہ گلوکوز حاصل کر کے زندہ رہتے ہیں۔
گلوکوز کا ہی ایک تیسرا پولی مر بھی ہوتا ہے جسے سیلولوز (Cellulose) کہتے ہیں۔ اس سے پودوں کے خلیات کی سب سے بیرونی دیوار (cell wall) بنی ہوتی ہے۔ جانوروں کے خلیات میں ایسی کوئی دیوار نہیں ہوتی۔ بدقسمتی سے انسان سیلولوز کو ہضم کر کے توانائی حاصل نہیں کر سکتا مگر گائے بکری اور دیگر چرنے والے جانوروں کے معدے میں خاص طرح کے جراثیم (Trichonympha) موجود ہوتے ہیں جو سیلولوز کو گلوکوز میں تبدیل کر دیتے ہیں جو ان جانوروں کی غذا بن جاتا ہے۔ دیمک کی آنتوں میں بھی ایسے ہی جراثیم موجود ہوتے ہیں۔ یہی وجہ ہے کہ دیمک لکڑی کھا سکتی ہے کیونکہ لکڑی کا لگ بھگ نصف حصہ سیلولوز پر مشتمل ہوتا ہے۔
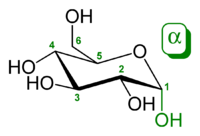 α-D-glucopyranose (chair form)
| |
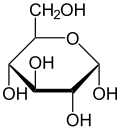 Haworth projection of α-D-glucopyranose
| |
 Fischer projection of D-glucose
| |
| نام | |
|---|---|
| Preferred IUPAC name
D-Glucose | |
| Systematic IUPAC name
(2R,3S,4R,5R)-2,3,4,5,6-Pentahydroxyhexanal | |
| دیگر نام
Blood sugar
Dextrose Corn sugar D-Glucose Grape sugar | |
| شناخت | |
| مخففات | Glc |
| CAS | 50-99-7 |
| بوب کیم (PubChem) | 5793 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| خواص | |
| ظہور | White powder |
| کثافت | 1.54 g/cm3 |
| نقطة الانصهار | 146 °س، 419 °ک 295 °ف |
| الذوبانية في الماء | 909 g/L (25 °C (77 °F)) |
| قابلية مغناطيسية | −101.5×10−6 cm3/mol |
| عزم جزيئي ثنائي القطب | 8.6827 |
| كيمياء حرارية | |
| الحرارة القياسية للتكوين ΔfH |
−1271 kJ/mol[1] |
| إنتروبيا مولية قياسية S |
209.2 J K−1 mol−1[2] |
| الحرارة النوعية، C | 218.6 J K−1 mol−1[2] |
| كود ATC | B05 |
| المخاطر | |
| NFPA 704 | |
| گلوکوز کا پولیمر | آئیسومر | مولیکیولی جوڑ[3] |
|---|---|---|
| نشاستہ (اسٹارچ) | الفا گلوکوز | ایک گلوکوز کا پہلا کاربن دوسرے گلوکوز کے چوتھے کاربن سے جُڑتا ہے۔ |
| گلائیکوجن | الفا گلوکوز | ایک گلوکوز کا پہلا کاربن دوسرے گلوکوز کے چھٹے کاربن سے جُڑتا ہے۔ |
| سیلولوز | بی ٹا گلوکوز | ایک گلوکوز کا پہلا کاربن دوسرے گلوکوز کے چوتھے کاربن سے جُڑتا ہے۔ |
انسانی جسم صرف ڈی گلوکوز استعمال کر سکتا ہے اور ایل گلوکوز بالکل استعمال نہیں کر سکتا۔ ڈی سے مراد dextro اور ایل سے مراد levo ہے۔ ڈی گلوکوز اور ایل گلوکوز کے درمیان ایسا ہی فرق ہوتا ہے جیسے دائیں ہاتھ اور بائیں ہاتھ کے دستانوں میں ہوتا ہے۔ کیمیا میں اسے isomer کہتے ہیں۔ اس کے برعکس انسانی جسم میں استعمال ہونے والے سارے امینو ایسڈ ایل قسم سے تعلق رکھتے ہیں۔
مزید دیکھیے
ترمیم
نگار خانہ
ترمیمالفا ڈی گلوکوز اور بی ٹا ڈی گلوکوز۔ یہاں کاربن کے ایٹموں کو کالے اور آکسیجن کے ایٹموں کو لال رنگ سے ظاہر کیا گیا ہے۔ سفید رنگ سے ہائیڈروجن کے ایٹم دکھائے گئے ہیں۔ ہر حلقے یا کڑی میں پانچ ایٹم کاربن کے ہیں جبکہ چھٹا ایٹم آکسیجن کا ہے۔
حوالہ جات
ترمیم- ↑ V. V. Ponomarev؛ L. B. Migarskaya (1960)، "Heats of combustion of some amino-acids"، Russ. J. Phys. Chem. (Engl. Transl.)، ج 34: 1182–83
- ^ ا ب Juliana Boerio-Goates (1991)، "Heat-capacity measurements and thermodynamic functions of crystalline α-D-glucose at temperatures from 10K to 340K"، J. Chem. Thermodynam.، ج 23 شمارہ 5: 403–09، DOI:10.1016/S0021-9614(05)80128-4
- ↑ "Starch, Glycogen and Cellulose"۔ 2018-07-04 کو اصل سے آرکائیو کیا گیا۔ اخذ شدہ بتاریخ 2018-08-20
